stampa | chiudi
Lunedì 20 FEBBRAIO 2023
Big Pharma spende di più in marketing che in ricerca. Lo studio sul BMJ: “Un trend che non giustifica i prezzi così alti dei farmaci innovativi”
Dal 1999 al 2018, le 15 maggiori società biofarmaceutiche hanno speso 2,2 trilioni di dollari per i costi di attività di vendita, generali e amministrative e1,4 trilioni di dollari su R&S” Ma i prezzi degli innovativi, e non solo, sono alle stelle, almeno negli Usa. LO STUDIO.
Un team di ricercatori guidati da Aris Angelis della London School of Economics analizzando i bilanci delle big pharma hanno scoperto che dal 1999 al 2018, le 15 più grandi aziende biofarmaceutiche del mondo hanno speso di più in attività di vendita, generali e amministrative che in ricerca e sviluppo.
La maggior parte di queste società, scrivono Angelis e colleghi sul British Medical Journal del 15 febbraio, ha anche speso di più per il riacquisto di azioni proprie e il pagamento di dividendi che per la ricerca e lo sviluppo.
Per i ricercatori se le grandi farmaceutiche rifocalizzassero la loro spesa potrebbero tra l’altro fornire farmaci più innovativi a prezzi accessibili.
E sì, perché alla fine, al di là della scelta di investire più in marketing che in ricerca, il problema centrale resta quello dei prezzi che negli Stati Uniti, come evidenziato nell’articolo sul BMJ, per quanto riguarda i farmaci da prescrizione appena lanciati sono aumentati da una mediana di circa $ 1400 all'anno (£ 1200; € 1300) nel 2008 a oltre $ 150.000 all'anno nel 2021.
Tra gli esempi citati dai ricercatori britannici quello di Onasemnogene abeparvovec (Zolgensma), una terapia genica approvata dalla FDA nel 2019 per l'atrofia muscolare spinale che, al momento dell'approvazione, diventò il farmaco più costoso di sempre, con un prezzo di oltre 2 milioni di dollari per un trattamento a singola dose.
Ma diversi farmaci più recenti per le malattie rare, scrivono ancora i ricercatori, hanno un prezzo ancora più alto, con una terapia genica per l'emofilia B approvata dalla FDA nel novembre 2022 che costa 3,5 milioni di dollari per dose.
E anche farmaci vecchi e comuni, sempre secondo Allison & C., hanno visto aumenti di prezzo “inspiegabili”.
Sempre negli Usa, per esempio, il prezzo di listino di alcuni prodotti insulinici è più che raddoppiato dal 2007 al 2018, mentre un rapporto del governo statunitense ha identificato 1.216 prodotti che avevano visto salire i prezzi sopra l'inflazione tra luglio 2021 e luglio 2022, con un incremento medio del 31,6%.
L'industria biofarmaceutica, ricordano gli autori dello studio, sostiene da tempo che sono necessari prezzi elevati per sostenere la ricerca e lo sviluppo (R&S) di nuovi farmaci.
E citano quanto dichiarò recentemente un alto dirigente di Johnson & Johnson al quale era stato chiesto di giustificare un prezzo di 10.000 dollari al mese per un farmaco per curare il cancro alla prostata: “Le malattie facili sono state in gran parte risolte. Diventa sempre più difficile man mano che cerchiamo nuovi trattamenti per malattie sempre più impegnative”.
Senza contare, scrivono ancora i ricercatori, che le compagnie farmaceutiche fanno spesso notare come i loro azionisti e investitori potrebbero facilmente trasferire i loro investimenti in altri settori più redditizi e meno rischiosi.
E in effetti, riconoscono Allison & C., “ci sono grandi rischi finanziari associati all'introduzione sul mercato di nuovi farmaci, poiché molte molecole candidate non ce la faranno perché sono inefficaci o dannose, o entrambe le cose”.
Tuttavia, rimarcano, “l'analisi della spesa e dei prodotti delle aziende farmaceutiche solleva interrogativi sull'affermazione secondo cui sono necessari prezzi elevati dei farmaci per sostenere un'innovazione di valore”.
Le norme contabili, scrivono, “rendono complicato il confronto tra i profitti dell'industria farmaceutica e di altre industrie, ma i dati suggeriscono che le aziende farmaceutiche sono particolarmente redditizie, anche dopo l'adeguamento per la spesa in R&S come quota dei ricavi”.
E che “sembra inoltre esserci uno scollamento tra i costi e i prezzi di ricerca e sviluppo dei prodotti, come rileva uno studio recente pubblicato su Jama, che non ha trovato alcuna associazione tra quanto le aziende farmaceutiche spendono in ricerca e sviluppo e i prezzi che fanno pagare per i nuovi farmaci”. 11
Secondo gli autori della nuova ricerca “la giustificazione dei prezzi elevati dei farmaci ignora anche i cospicui investimenti pubblici nella scoperta e nello sviluppo di farmaci, che hanno contribuito alla ricerca di base e traslazionale alla base di tutti i nuovi farmaci approvati dalla FDA dal 2010 al 2016”. Senza contare che “più di un quarto dei nuovi farmaci approvati dalla FDA dal 2008 al 2017 erano legati a investimenti pubblici durante le ultime fasi di sviluppo”.
“Ciò significa, osservano Allison & C, “che la società sta potenzialmente pagando due volte per i nuovi farmaci, prima sotto forma di ricerca sovvenzionata con fondi pubblici e poi attraverso gli alti prezzi dei prodotti”.
La maggior parte della spesa del settore non è in ricerca e sviluppo
Sulla base dei rapporti finanziari pubblicamente disponibili dal 1999 al 2018, i ricercatori segnalano che le 15 maggiori società biofarmaceutiche hanno registrato un fatturato totale di 7,7 trilioni di dollari.
Durante questo periodo, sottolineano, “hanno speso 2,2 trilioni di dollari per i costi di attività di vendita, generali e amministrative - una categoria che include marketing e pubblicità, nonché quasi tutti gli altri costi aziendali non direttamente attribuibili alla produzione di un prodotto o alla prestazione di un servizio - e1,4 trilioni di dollari su R&S”.
Entrate totali, spese di vendita, generali e amministrative e spese di ricerca e sviluppo (miliardi di dollari) per le 15 maggiori aziende biofarmaceutiche, 1999-2018.
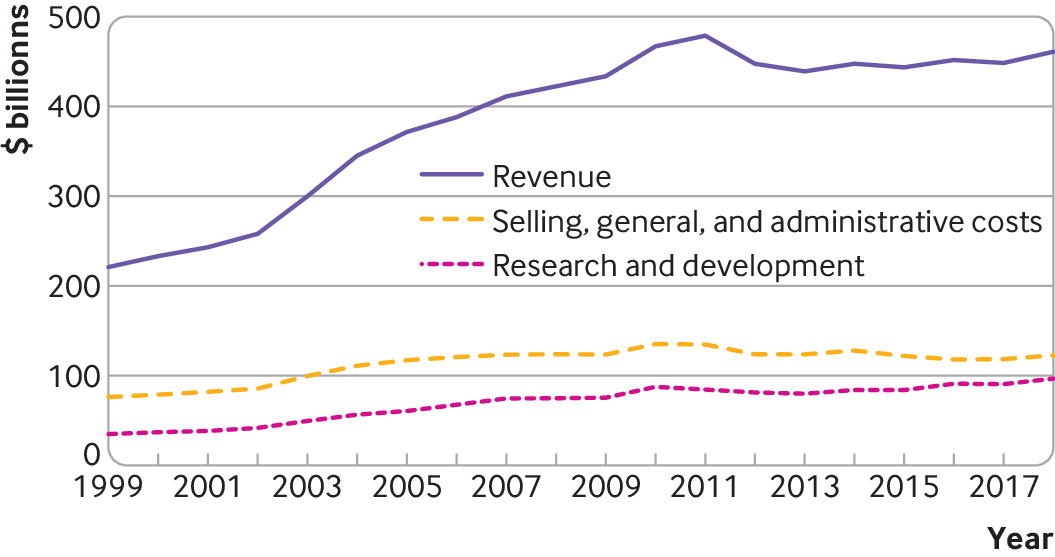
Note: Dati ricavati dai moduli annuali e trimestrali delle società statunitensi depositati presso la Securities and Exchange Commission degli Stati Uniti e dai rapporti finanziari annuali delle società non statunitensi.
I dettagli precisi di ciò che è incluso nelle attività di R&S e di vendita, generali e amministrative, osservano però i ricercatori, “possono non essere chiari”.
Ad esempio, spiegano, “le aziende possono condurre sperimentazioni di marketing (seeding trial) di farmaci appena approvati considerandole parte della spesa in R&S dichiarata, ma tali trial hanno uno scarso o nullo impatto scientifico” e possono essere considerati parte integrante delle “strategie di marketing”.
Ma in ogni caso, considerando anche queste varianti per gli autori dell’articolo sul BMJ, “è chiaro che dal 1999 al 2018 le aziende hanno speso di più per le attività di vendita, generali e amministrative che per la ricerca e lo sviluppo, in linea con quanto già accaduto dal 1975 al 2007”.
Un altro fattore, rimarcato da Allison & C, è quello che vede la maggior parte delle stesse società “spendere di più per l'acquisto delle proprie azioni che per la ricerca e lo sviluppo durante questo periodo”, a tutto vantaggio degli alti dirigenti aziendali, il cui reddito è spesso direttamente collegato al prezzo delle azioni.
Un'indagine sui prezzi dei farmaci condotta dalla Commissione per la supervisione e la riforma della Camera degli Stati Uniti, citata nel lavoro del BMJ, ha mostrato che, dal 2016 al 2020, le 14 maggiori aziende farmaceutiche hanno speso 577 miliardi di dollari in riacquisti di azioni proprie e dividendi - 56 miliardi di dollari in più rispetto alla ricerca e sviluppo - in un momento in cui la retribuzione annuale dei dirigenti è cresciuta del 14%”.
Questa tendenza, notano gli autori, “riflette la crescente finanziarizzazione dell'industria farmaceutica negli ultimi decenni, che si è generalmente concentrata sulla massimizzazione del valore per gli azionisti”.
In ogni caso, lo segnalano gli stessi autori, “sebbene negli ultimi vent'anni le aziende abbiano speso di più per le attività di vendita, generali e amministrative e per il riacquisto di azioni proprie che per la ricerca e lo sviluppo, le spese di vendita, generali e amministrative (come quota delle entrate) sono scese dal 35% al 27% in questo periodo mentre la spesa in R&S è aumentata dal 16% al 21%”.
E va anche registrato che “le aziende farmaceutiche si impegnano in fusioni e acquisizioni per accedere a nuovi prodotti promettenti” e che oggi “le grandi aziende farmaceutiche non sono coinvolte nella scoperta della maggior parte dei nuovi farmaci” e che ciò suggerisce “uno spostamento della strategia dalla fase iniziale di ricerca e scoperta all'acquisizione e allo sviluppo in fase avanzata”.
“Molte esigenze sanitarie rimangono insoddisfatte dall'attuale modello di business farmaceutico”, scrivono i ricercatori e “ciò include malattie trascurate (neglectded diseases), resistenza antimicrobica e altre malattie infettive emergenti”.
Senza contare poi che “in molti mercati importanti l'attuale sistema premia i nuovi prodotti indipendentemente dai vantaggi comparativi o dal contributo alle priorità di salute pubblica, il che riflette in parte il fatto che le autorità di regolamentazione valutano i nuovi farmaci in base al loro rapporto rischio-beneficio individuale piuttosto che mostrare un valore clinico aggiunto”.
“Inoltre, osservano ancora gli autori, i brevetti vengono assegnati sulla base della novità chimica e dell'inventiva del prodotto, indipendentemente dal valore terapeutico aggiunto”.
Indirizzare l'innovazione al servizio degli obiettivi di salute pubblica
Per Allison & C. “considerando l’importo speso per le attività non di ricerca e sviluppo e che la maggior parte dei nuovi farmaci aggiunge poco o nessun valore terapeutico, in teoria l'industria biofarmaceutica potrebbe generare innovazione di maggior valore medico con le sue risorse esistenti”.
E che “non dovrebbe essere necessario trasferire i costi di ricerca e sviluppo sui pazienti e sui sistemi sanitari attraverso prezzi sempre più alti e inaccessibili”, anche se, concludono, “è improbabile che ciò accada senza l'intervento o la regolamentazione del governo lungo il ciclo di vita dei nuovi farmaci”.
Ma cosa dovrebbero fare i Governi e le agenzie regolatorie? Cinque le mosse indicate dal BMJ:
- Rendere i sistemi brevettuali nazionali più rigorosi per evitare di premiare l’innovazione indipendentemente dal valore terapeutico aggiunto.
- Comunicazione chiara da parte delle autorità sanitarie pubbliche per delineare le priorità di ricerca e sviluppo focalizzate sui bisogni sanitari e l'uso strategico dei finanziamenti pubblici per la ricerca per sostenerli.
- Allocazione più intelligente dei fondi per la ricerca pubblica con mantenimento della proprietà (parziale) che può essere sfruttata per perseguire obiettivi di salute pubblica, compresi prezzi accessibili.
- Innalzamento degli standard di prova per l'autorizzazione all'immissione in commercio, richiedendo alle aziende di condurre studi clinici comparativi progettati per stabilire un valore terapeutico aggiunto.
- Riformare i sistemi di determinazione dei prezzi e dei rimborsi per premiare le aziende che sviluppano farmaci che offrono benefici clinici e scoraggiare le strategie me-too e evergreen.
Per le aree terapeutiche in cui gli incentivi di mercato sembrano inadeguati, come gli antibiotici per le infezioni resistenti ai farmaci, aggiungo gli autori, “potrebbe essere necessaria una serie completa di incentivi per i produttori”.
“Una maggiore trasparenza sui prezzi dei farmaci, sullo stato dei brevetti, sui costi di ricerca e sviluppo e sui dati delle sperimentazioni cliniche, come raccomandato in una risoluzione dell'Assemblea mondiale della sanità del 2019, potrebbe aiutare a ridefinire il contratto sociale tra le parti interessate coinvolte nello sviluppo dei farmaci e allineare gli incentivi agli obiettivi di salute pubblica”, scrivono ancora Allison & C. che ricordano anche quanto affermato dal Consiglio dell'OMS sull'Economia della Salute per Tutti nel 2021, quando venne sancito che “le politiche economiche, fiscali e industriali che governano il settore devono essere riprogettate per migliorare i risultati sanitari e garantire che l'innovazione sanitaria sia per il bene comune”.
Cesare Fassari